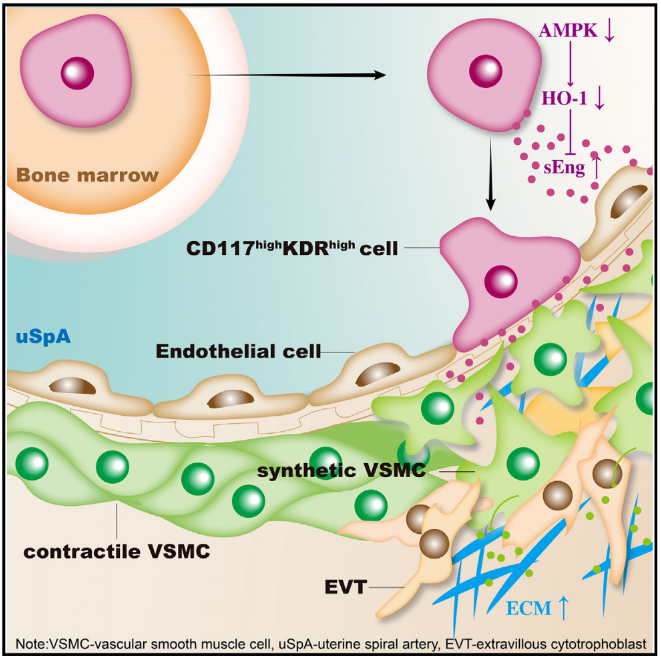
子宫螺旋动脉重铸对子宫-胎盘循环的建立至关重要,此过程异常是造成胎盘源性疾病的关键病因。子痫前期(Preeclampsia, PE)是威胁母体和胎儿健康的严重妊娠期并发症,主要分为早发型和晚发型两种亚型。早发型PE(妊娠34周前出现PE临床表现)与子宫螺旋动脉重铸过程异常有关。子宫螺旋动脉重铸初始阶段,子宫自然杀伤(Uterine natural killer, uNK)细胞和绒毛外滋养细胞 (Extravillous cytotrophoblasts, EVTs) 渗透至蜕膜中,逐渐侵袭子宫螺旋动脉使其重塑为高排低阻的血管以维持子宫-胎盘循环。构成子宫螺旋动脉血管壁的血管平滑肌细胞(Vascular smooth muscle cells, VSMCs)在重塑过程中经历去分化、合成细胞外基质(Extracellular matrix, ECM)等过程,以维持重铸后血管的完整性;若重铸过程中管腔扩张受限,且ECM过度沉积于重铸血管壁中,那么重铸后子宫动脉将出现脉粥样硬化样改变,导致血管反应性低,血流灌注不足等不良结局。内皮祖细胞(Endothelial progenitor cells, EPCs)是一类参与血管损伤修复的低分化潜能细胞,鉴于子宫螺旋动脉重铸本质上是一个血管损伤后再修复过程,故本研究提出假设:EPCs在子宫螺旋动脉重铸过程中发挥重要的调控作用,继而影响子宫-胎盘循环的建立。
2024年4月24日,重庆医科大学附属第一医院主治医师谭彬博士(与重庆医科大学附属妇女儿童医院博士后林俐为共同一作)、童超教授和重庆医科大学附属妇女儿童医院漆洪波教授团队在Developmental Cell上发表了文章Endothelial progenitor cells control remodeling of uterine spiral arteries for the establishment of utero-placental circulation,揭示了内皮祖细胞影响子宫螺旋动脉重铸调控子宫-胎盘循环的建立。