
医学界在肝硬化治疗领域取得重要进展,我国科学家首次揭示了干细胞如何通过调节免疫系统来帮助改善失代偿期肝硬化患者的健康状况。
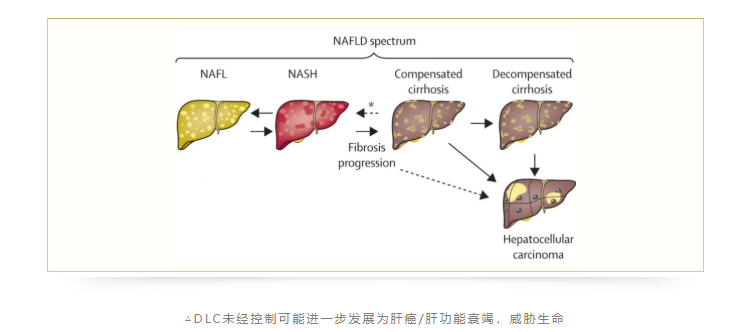
肝硬化是一种常见的慢性肝病,当疾病进展到失代偿期(DLC)时,患者的肝脏功能已出现明显衰竭,无法维持机体正常的生理需求。
此时常伴随腹水、食管静脉曲张、肝性脑病等严重并发症,患者面临着极高的死亡风险。
在全球范围内,肝硬化患者数量庞大。据数据显示,全球约有1060万失代偿期肝硬化患者,他们五年生存率仅在19%-35%之间。
长期以来,肝移植被认为是唯一能根治的手段,但受限于供体短缺、手术风险和高昂成本,最终能受益的患者不足1%。
发掘新疗法的道路上,间充质干细胞(MSC)因易于获取、低免疫原性、分化潜能和强大的免疫调节能力被医学界寄予厚望,此前一些研究也显示出干细胞具有改善肝硬化症状的潜力,是该领域冉冉升起的新星。
而为了促进临床转化,中国科学院院士王福生及其研究团队多年深耕于干细胞治疗肝硬化的临床研究,近日,他们于国际顶级期刊《Signal Transduction and Targeted Therapy》(影响因子:52.7)发表最新论文——首次在人体临床试验(Ia/Ib 期)中阐明MSC治疗DLC的安全性、剂量-效应关系及核心免疫调节机制,为后续更大规模的临床应用奠定了重要基础。

干细胞疗法:
肝病治疗新研究揭示机制奥秘
近年来,间充质干细胞(MSC)疗法作为一种新兴的治疗策略逐渐受到关注。这类细胞因其易于获取、免疫原性低、分化潜能大以及具有免疫调节能力,被认为是具有前景的细胞治疗候选细胞。
免疫调节能力是间充质干细胞(MSC)的“绝技”之一,它被证实能调节先天免疫和适应性免疫,如MSC可以诱导CSF-1R +单核细胞产生IL-10,并通过Pinch-Cxcl12-Mbl2 axis41调节单核细胞驱动的炎症。
但这些机制见解基本来自于临床前研究,人体实验的证据有限,与此同时,人体的最佳给药策略和剂量依赖性治疗机制也是一团迷雾,这限制了干细胞疗法的发展与应用。
王福生院士尝试揭开这些谜题,研究团队通过精心设计的I期临床试验,采用“3+3”剂量递增方案,对24例中重度失代偿性肝硬化患者进行了系统性评估。
试验分为两个阶段:Ia期单剂量试验和Ib期多剂量试验。研究发现间充质基质细胞治疗安全可耐受,即使在高剂量和多次输注情况下,患者未出现严重相关不良反应。
在机制研究方面,研究团队取得了三项重要发现:
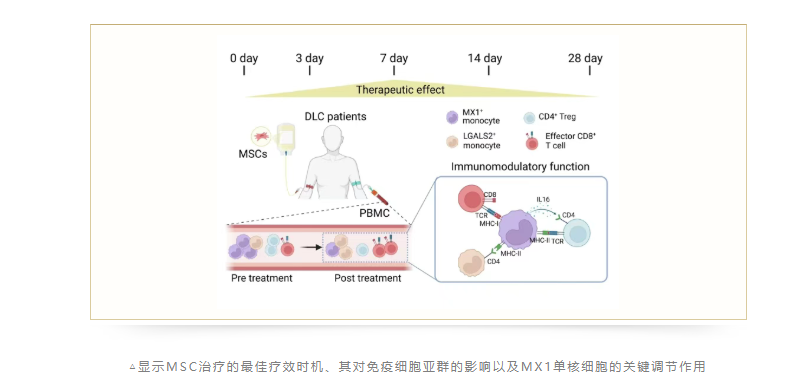
首先,首次在人体内鉴定出MX1+单核细胞是介导MSC免疫调节功能的关键细胞亚群。间充质基质细胞通过剂量依赖性地降低MX1+单核细胞比例及其促炎功能来发挥治疗作用。
其次,间充质基质细胞免疫调节效应在输注后第7天达到峰值,到第14天减弱,这为设计多次给药间隔方案提供了关键理论依据。
第三,MX1+单核细胞比例的变化与临床结局相关,有望成为预测MSC治疗反应的新型生物标志物,用于未来临床试验治疗优化。
研究结果显示,MSC治疗安全可耐受,即使在高剂量和多次输注情况下,患者未出现严重相关不良反应。
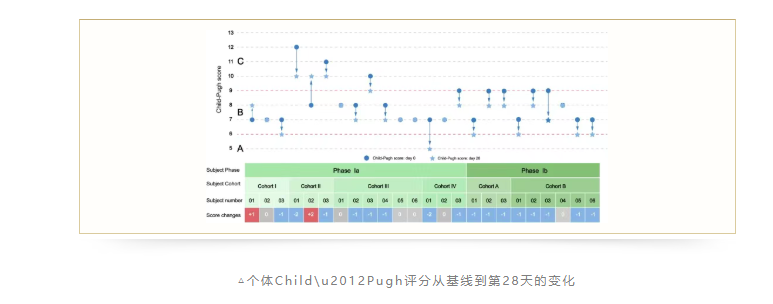
还发现包括肝功能指标Child-Pugh评分、生活质量等出现剂量依赖的临床改善信号。
高剂量组(2.0×10⁸细胞)88.9%的患者Child-Pugh评分降低,显著优于低剂量组(53.3%)。多重输注组肝功能指标(白蛋白、前白蛋白)改善率超85%。
生活质量方面,慢性肝病问卷(CLDQ)评分改善率达88.9%。这些数据为干细胞治疗肝硬化的效果提供了有力证据。
写在最后
随着后续更大规模临床试验的开展,间充质干细胞疗法有望成为对抗终末期肝病、改善患者预后的重要治疗选择。
未来科学家将继续探索干细胞疗法在不同疾病领域的应用潜力,为更多患者带来希望。
请注意:本文旨在介绍医学研究进展,不可作为医疗建议。实际治疗方法请咨询专业医疗机构和执业医师。
参考资料: [1]Dose-escalation studies of mesenchymal stromal cell therapy for decompensated liver cirrhosis: phase Ia/Ib results and immune modulation insights.https://www.nature.com/articles/s41392-025-02318-4#Sec1
欢迎关注微信公众平台:重庆铂而斐
免责声明: 我们尊重原创,也注重分享,不作商业用途,不作医疗建议,仅作交流学习。版权归原作者,如有侵权敬请谅解,请联系我们删除。